国家药监局发布仿制药参比制剂目录
来源:医美查
2022年05月20日
5月19日,国家药品监督管理局发布通告,经国家药品监督管理局仿制药质量和疗效一致性评价专家委员会审核确定,国家药监局发布了仿制药参比制剂目录第五十四批。
附件提到,目录中所列尚未在国内上市品种的通用名、剂型等,以药典委核准的为准。参比制剂目录公示后,未正式发布的品种将进行专题研究,根据研究结果另行发布。选择未进口参比制剂开展仿制药研究除满足其质量要求外,还需满足现行版《中国药典》和相关指导原则要求。
放射性药物不同于普通化学药物,具有一定的特殊性如放射性、时效性、按放射性活度给药等特点,参比制剂主要用于明确其研发目标和基本要求,可根据其药物特性同时结合参比制剂的可获得性进行研究。

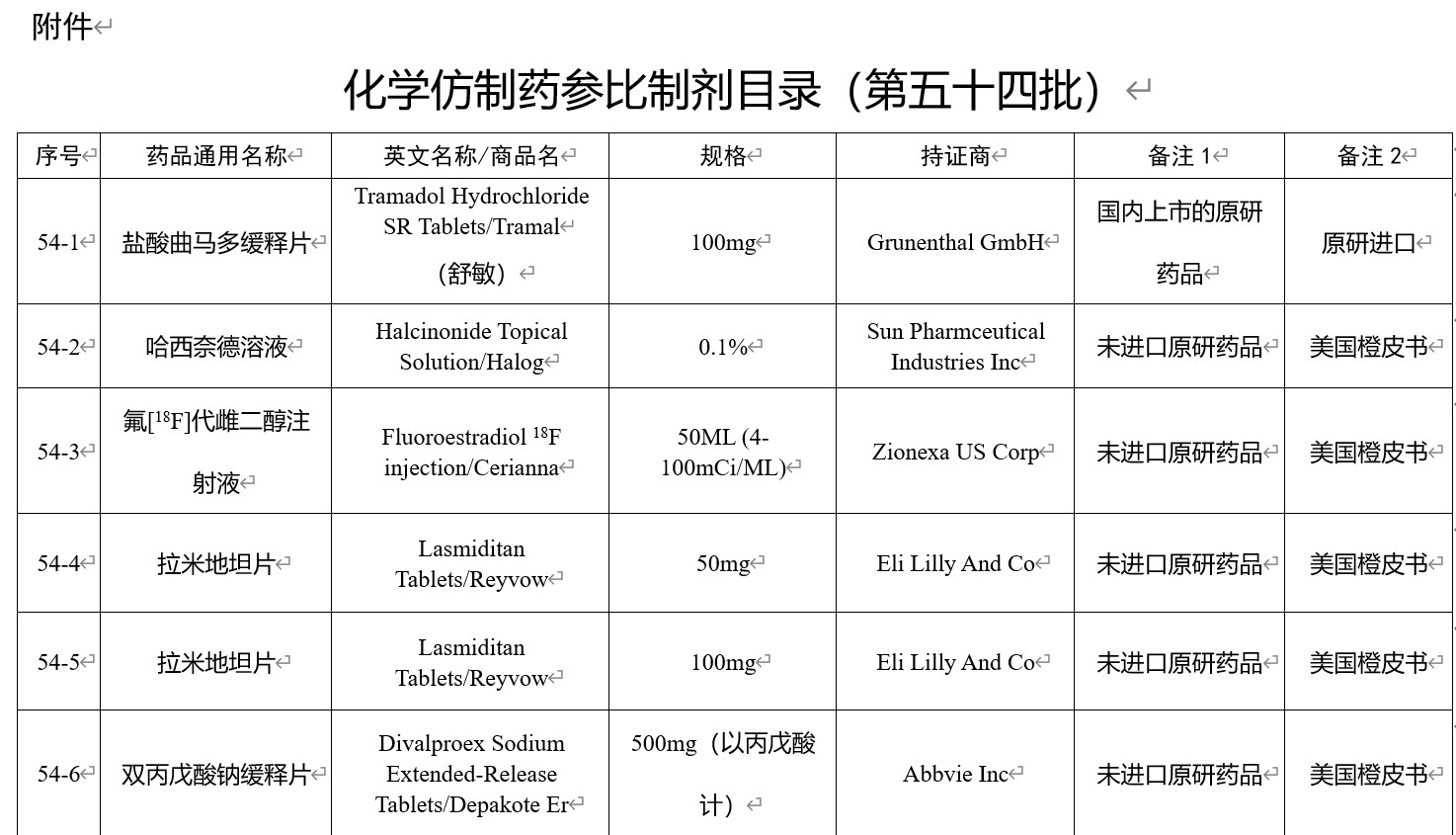
图片来源:国家药监局官网
下载医美查APP
了解更多信息
相关资讯:
万联证券首予爱美客买入评级 “轻医美”当道爱美客增长空间广阔
国家药监局发布《抗肿瘤治疗的免疫相关不良事件评价技术指导原则》
医美 | 爱美客:国内医美行业龙头的进阶"三步曲"
国家药监局批准注册212个医疗器械产品
医美 | 半岛医疗:光电医美行业"领跑者"又一新品获批
5.15医美充电宝 | 药品管理法实施条例(修订草案征求意见稿)发布;税务稽查瞄准医美行业,追缴税款达千万元
美周关注NO.12丨华东医药全球战略新布局;某机构漏税被判千万罚款
医美 | 胶原蛋白:国内已获批的4款"胶原蛋白"填充剂大比较
忽然一周|华东医药:拟增加经营范围“易制毒化学品”;四环医药否认被华润集团私有化;福州一机构杜撰医生信息、卖过期药被罚30万元
医美行业首个细分新原料,吸金家族又添“大将”
相关报价:
热门话题:
国家药监局
国家药品监督管理局







